Cinética Actividad: ¿Cómo ocurren las reacciones - EducarChile
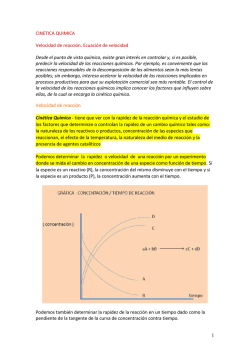
Nivel: 3º Medio Subsector: Ciencias químicas Unidad temática: Cinética Actividad: ¿Cómo ocurren las reacciones químicas? ¿Qué es la cinética de una reacción química? La cinética de una reacción química da cuenta de la velocidad con la que ocurre Esta reacción y de qué forma reaccionan los reactivos para formar un producto. ¿Cómo ocurren las reacciones químicas? ¿Cómo es que los reactivos se juntan, reaccionan, se mezclan, se unen o se separan para formar un producto distinto al inicial? ¿Qué es lo que tiene que ocurrir? ¿Un reactivo cualquiera pasa por varias etapas para formar un producto o sólo se transforma “mágicamente” en un producto nuevo? ¿Cómo lo hace? ¿Qué se necesita? Las respuestas a estas preguntas las podemos encontrar en dos teorías que son complementarias. Ambas intentan explicar cómo ocurren las reacciones químicas. La Teoría de colisiones indica que las reacciones se producen a través de choques entre las partículas de reactivo, y la Teoría del complejo activado indica que los reactivos alcanzan un estado de transición de alta energía llamado complejo activado, el que luego decae a productos estables. Por medio de esta actividad aprenderás en qué consisten ambas teorías, cómo funcionan y cómo dos o más reactivos dan lugar a un producto. Preguntas y aplicaciones Realiza una investigación sobre las teorías anteriormente presentadas. Busca información en tu texto de estudios o en las fichas temáticas del portal educarchile. Este cuestionario será evaluado la próxima clase en forma de interrogación al azar. Puedes comenzar leyendo acerca de cinética química y luego basarte en las siguientes preguntas para poder comprender ambas teorías. I. Teoría de colisiones 1) ¿En qué consiste la Teoría de colisiones? __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ 1 2) ¿Qué es un choque ineficaz y qué uno eficaz? __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ _________________________________________________________________________ 3) ¿Cómo afectaría el aumento de presión y de temperatura sobre el número de colisiones entre partículas de reactivo? __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ _________________________________________________________________________ 4) Observa la animación “Choques” que se encuentra en el portal Educarchile. En ella se ilustran un choque eficaz y otro ineficaz. 5) Escribe pequeñas conclusiones que te permitan describir en pocas y con tus palabras en qué consiste esta teoría. __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ Actividad para desarrollar en parejas. II. Teoría del complejo activado 1) ¿En qué consiste la Teoría del complejo activado? __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ 2) ¿Qué es la energía de activación? __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ 2 3) ¿Qué ocurre con la velocidad de una reacción si ésta requiere de poca energía de activación? __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ 4) ¿Qué ocurre con la velocidad de una reacción si ésta requiere de mucha energía de activación? __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ 5) ¿Qué es complejo activado? __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ 6) ¿Qué es una reacción exotérmica? __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ 7) ¿Qué es una reacción endotérmica? __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ 8) Para una reacción cualquiera: A+B C+D a) Dibuja un diagrama de energía si la reacción es exotérmica. b) Dibuja un diagrama de energía si la reacción es endotérmica. 9) Escribe pequeñas conclusiones que te permitan describir con tus palabras en qué consiste esta teoría. __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ __________________________________________________________________________ 3
© Copyright 2026