OH OH Cl OH Br Br OO OH OH OH OH OH i) ii) iii) iv) v) vi) vii) viii
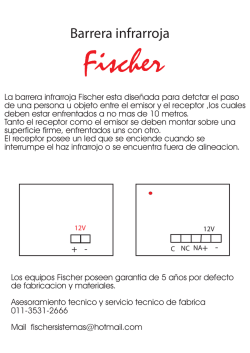
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CC.QQ. Y FARMACIA DEPARTAMENTO DE QUIMICA ORGANICA QUIMICA ORGANICA I – 2016 - SECCION “D” Elaborado por Licda. Nora Guzmán TAREA No. 10 Instrucciones: Resuelva grupalmente los siguientes ejercicios. Fecha de entrega: martes 3 de mayo de 2016. 1. Mediante un * indique los centros estereogénicos en los siguientes compuestos: OH OH i) OH Cl ii) iv) iii) OH viii) v) vi) OH O HO vii) HO Br Br O OH 2. Sólo uno de los dos isómeros estructurales de fórmula C4H10O tiene un átomo asimétrico. Cuál es su estructura? Dibuje las proyecciones de Fischer de los dos enantiómeros y asigne configuración absoluta. 3. De acuerdo a las Reglas de Cahn, Ingold y Prelog, indique cuál miembro de cada pareja tiene la mayor prioridad. a) Cl- ó HOCH2- b) (CH3)2CH- ó BrCH2- c) ClCH2CH2- ó H2NCH2CH24. A continuación aparece la estructura de uno de los enantiómeros de carvona el cuál corresponde a la (+)-carvona presente en la semilla de la alcaravea a. Identifique el átomo asimétrico empleando * y determine su configuración absoluta. b. Dibuje la fórmula de cuñas de su correspondiente enantiómero, el cual se encuentra en el aceite de hierbabuena, responsable de su fragancia. c. Si tuviera los dos enantiómeros de la carvona en botellas no etiquetadas, ¿podría utilizar únicamente su nariz y un polarímetro para determinar c.1 Si es el enantiómero (+) o (-) el que huele a hierbabuena? c.2 Si es el enantiómero (R) o (S) el que huele a hierbabuena? c.3 En base a las fórmulas de cuñas con que cuenta, indique qué más información puede añadir a los incisos c.1 y c.2 5. Compruebe respecto al estereoisómero (a) del 2-amino-1-propanol si (b), (c) y (d) son idénticos a él o si corresponden a su enantiómero. Asigne configuración absoluta de (a). NH2 H CH3 (a) CH3 HOCH2 H (b) CH3 CH2OH NH2 CH2OH H2N H NH2 HOCH2 CH3 (c) 6. Dibuje para cada uno de los siguientes compuestos la fórmula de cuñas (donde dos de los sustituyentes coinciden con el plano) para el respectivo enantiómero complementario y asigne configuración absoluta para ambos miembros de cada par enantiomérico. H (d) F COOH Cl H NH2 H Br CH3 (a) (b) 7. Dibuje las proyecciones de Fischer y fórmulas de cuñas del confórmero eclipsado de los posibles estereoisómeros del 3-bromo-2-butanol, CH3CH(OH)CH(Br)CH3, indicando para cada uno el respectivo nombre IUPAC que identifique configuracionalmente a cada estereoisómero. Muestre sus mutuas relaciones como estereoisómeros configuracionales (enantiómeros, diasterómeros). 8. Para la siguiente fórmula, HOOCCHBrCHBrCOOH : a. ¿Cuántos estereoisómeros podrían plantearse teóricamente? b. Dibuje las respectivas proyecciones de Fischer, fórmulas de cuñas y proyecciones de Newmann (en ambos casos del confórmero eclipsado), indicando para cada una de las primeras la configuración absoluta de cada centro quiral. c. Señale las relaciones de enantiomería y diasteromería. d. ¿Cuántos esteroisómeros diferentes tienen existencia real en este caso? Para contestar esto, tome en cuenta que el giro de 180° sobre el plano de uno de los esteroisómeros dibujados en (b) lo transforma en un compuesto idéntico a otro de los mismos estereoisómeros. Asigne la denominación general que se da a este tipo de esteroisómero y describa su actividad óptica. e. Explique con cuáles estereoisómeros de (b) podría preparar una mezcla racémica, indicando las condiciones de concentración relativa. 9. Dibuje las proyecciones de Fischer de: a) meso-3,4-hexanodiol b) (R)-2-aminobutano c) (2S, 3R)-3-amino-2-butanol 10. Si la D-galactosa tiene la siguiente estructura, dibuje la proyección de Fischer de la L-galactosa e indique la configuración absoluta de cada centro quiral. CHO H OH HO H HO H H OH CH2OH D-galactosa Al hacerse reaccionar la D-galactosa con NaBH4, esta se reduce a D-galactitol, donde no se observa respecto de la D-galactosa ningún cambio conformacional, mientras que el grupo –CHO se reduce a –CH2OH. Dibuje la proyección de Fischer del D-galactitol e indique cómo se mostrará la actividad óptica de dicho estereoisómero. NG/ng
© Copyright 2026