a) Modelo atómico de Dalton: Con este modelo propuesto
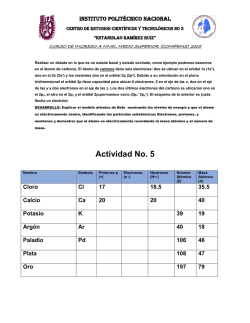
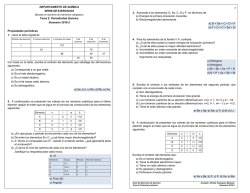
1 LICEO POLITÉCNICO BELÉN SECTOR DE QUIMICA PROF. KAREN BARRERA TAPIA Guía de Aprendizaje Química 3ºmedio Aprendizajes esperados: Valorar la importancia del trabajo científico en la construcción del modelo atómico actual. - Principales teorías atómicas: a) Modelo atómico de Dalton: Con este modelo propuesto entre los años 1803 y 1808 se inició el estudio del átomo. Su esquema es simple, enunciado por tres postulados: 1.- Cada elemento químico se compone de partículas muy pequeñas e indivisibles llamadas átomos. En todos los procesos químicos el número de átomos de cada elemento permanece constante. 2.- Todos los átomos de un elemento dado tienen masa y propiedades iguales, pero son distintos de los átomos de los demás elementos. 3.-En los elementos químicos los átomos de elementos diferentes están unidos entre sí en proporciones numéricas simples. b) Modelo atómico de Thomson: JJ Thomson, en 1897, fue el primero en proponer un modelo estructural interno del átomo. Utilizó en sus experimentos un tubo de descargas conocido también como tubo de Crookes. Éste consiste en un tubo de vidrio con electrodos metálicos en sus extremos, conectados a una fuente de energía de corriente continua. Al hacer vacío se observa la emisión de luz, que viaja desde el cátodo (polo negativo) hacia el ánodo (polo positivo). Como la luminosidad provenía del cátodo se les denominó rayos catódicos. Thomson colocó una cruz de malta dentro del tubo y observó que producía sombra. Con ello dedujo que el haz de luz está compuesto de partículas. A su vez sometió a dicho haz a un campo eléctrico y magnético y notó que sufría desviación hacia el polo positivo, dando prueba de su caga eléctrica negativa. Llamó a dicha partícula electrón. En 1886, Eugene Goldstein observó que al trabajar con un tubo de descarga de cátodo perforado, en dirección opuesta a los rayos catódicos, se desprendía una radiación. Estos rayos fueron designados rayos canales y resultaron ser partículas positivas, originadas por el choque de los rayos catódicos con átomos de gases residuales en el tubo. Con este experimento se estableció la existencia del protón. c) Modelo atómico de Rutherford: En 1911, Ernest Lord Rutherford y sus colaboradores Hans Geiger y ErnestMardsen, utilizando un haz de radiación alfa (radiación nuclear), bombardearon láminas muy delgadas de oro, colocando una pantalla de sulfuro de Zinc a su alrededor. Al revisar sus observaciones se lee: "de todas las partículas alfas proyectadas, la gran mayoría pasó sin problemas, pero otras sufrieron desviación". Debido a esto, Rutherford sugirió que el átomo ya no era una estructura compacta. Comprobó que la mayor parte de la masa del átomo estaba al centro, al que llamó núcleo. Éste estaba formado por protones y los electrones girando alrededor y entre ellos había una distancia, dado que las partículas alfa pasaban sin problemas. 2 Presenta sus estudios en 1911. En 1908 recibe el premio Nobel de Química. El modelo atómico de Rutherford también es conocido como el modelo planetario, debido a su semejanza con el sistema solar. Rutherford supone la existencia de otra partícula en el núcleo pero no lo demuestra. Quien sí comprueba tal supuesto de Rutherford es James Sir Chadwick, físico británico (1891-1974). Él ocupa la llamada cámara de niebla y en la reproducción observa que una partícula retrocedía. Ésta resultó tener carga eléctrica cero y poseer una masa igual a la del protón. A esta partícula se le conoce como neutrón. Dicho descubrimiento ocurre en el año de 1932 y en 1935 recibe el premio Nobel de Física. Con ello se demuestra que el átomo no es la partícula más pequeña sino que dentro de ella hay otras aún más pequeñas, las cuales nuevamente agrupadas dan origen al átomo. El átomo entonces está compuesto por protones, neutrones y electrones. - Modelo Atómico de Bohr El modelo de Rutherford distingue un núcleo, formado por protones y neutrones y una envoltura que son los electrones. Sin embargo, este modelo no da información de cómo se distribuyen los electrones ni explica el hecho de que los átomos emitan o reciban energía. Fue Niels Bohr (1885-1962) quien propone una mejora al modelo de Rutherford. Él argumentó lo siguiente: "dado que estamos en presencia de partículas, las cuales presentan carga eléctrica, necesariamente debe producirse una atracción entre ellas". Por lo tanto, el núcleo ejercerá atracción sobre el electrón, a tal punto de que el electrón empezará a proyectarse rápidamente al núcleo con la consecuencia de destruirlo. Esto no podía ser. El átomo es eterno, eso estaba claro. 1. Existen niveles de energía permitidos, que van de n igual uno a infinito. 2. Hay órbitas estacionarias en la cuales se mueve el electrón. No se manifiesta energía en estas órbitas. 3. El electrón podrá saltar de un nivel a otro de energía, sólo si se le entrega un cuantum de energía, expresado en valores enteros y no en fracciones. 4. Cuando el electrón pasa de un nivel menor a uno mayor de energía, ese proceso se llama absorción. Si va de uno mayor a uno menor, se llama emisión. 5. Para que ocurra ese salto entre los niveles deberá procurar una frecuencia tal que concuerde con esa diferencia energética. - Modelo Mecánico Cuántico El Modelo Mecánico Cuántico es la explicación actual sobre el comportamiento del átomo, fue desarrollado entre los años 1924 y 1927 por varios científicos. Quien inicia este modelo fue Louis de Broglie, quien intuyó que los electrones deberían tener el comportamiento de una onda. Esto fue demostrado en 1927. Esta particular conducta de los electrones implica la imposibilidad de determinar simultáneamente y con igual exactitud la posición y la velocidad de éstos, pues para conocerlas se debe interactuar con esta partícula. Este postulado se conoce con el nombre de Principio de Incertidumbre y fue enunciado en 1927 por Werner Heisenberg. Dado que el electrón es una partícula que presenta propiedades de onda, su movimiento pudo ser descrito por medio de una ecuación de onda. Erwin Schrödinger, en 1926, empleó las ideas de Broglie para llegar a una ecuación de onda que podría aplicarse al átomo de hidrógeno. La resolución de la ecuación de Schrödinger difiere de las ecuaciones simples, puesto que es una ecuación diferencial. Una de las características de éstas es el gran número de soluciones posibles. Los resultados obtenidos para el átomo de hidrógeno se pudieron extender con éxito al resto de los elementos del sistema periódico. 3 Actividad 1 Respecto a los modelos atómicos precursores del modelo actual, completa el siguiente cuadro comparativo de sus estructuras Las partículas fundamentales del átomo. Las partículas fundamentales que constituyen el átomo son los protones, con carga eléctrica positiva; los neutrones, sin carga eléctrica y; los electrones, con carga eléctrica negativa. Los protones y los neutrones se encuentran en el núcleo, tienen una masa muy similar (1,6725 . 10-24 grs, y 1,6749 . 10-24 grs. ), mientras que el electrón se encuentra en la corteza y tiene una masa muy pequeña. ( 9,1095 . 10-28 grs.), una masa1836 veces menor que la masa de un protón y un neutrón. 12.- Completa la información solicitada en la siguiente tabla. Actividad 2 Completen la siguiente tabla indicando los aportes de cada uno de los científicos para construcción del actual modelo atómico: Científicos John Dalton Aportes J. J. Thomson Ernest Rutherford Eugen Goldstein Robert Millikan JamesChadwick Niels Bohr El número atómico y el número másico. El número atómico de un elemento químico se simboliza con la letra Z y representa el número de protones contenidos en el núcleo. Además es la propiedad que identifica al elemento, así un elemento se caracteriza por su número atómico y si el átomo es neutro, este valor coincide con el número de electrones. Por ejemplo, el número atómico del Na es 11, entonces este átomo tiene 11 protones en su núcleo. Z = p+ 4 El número másico ó número de masa se simboliza con la letra A y representa la cantidad de protones y neutrones que hay en el núcleo; por lo tanto: A= Z + n A = p+ O bien: + n (n = neutrones) Como el número atómico (Z) representa el número de protones del átomo, el número de neutrones será: n = A - Z Recuerda que el número de masa siempre es un número entero, por eso a veces se debe aproximar. Para representar estas dos propiedades se utiliza la siguiente notación: A A X Z Z= = número de masa X= Símbolo del elemento número atómico Por ejemplo, para el sodio (Na), el número atómico (Z) es 11 y el número de masa es 23 y se anota de la siguiente manera: Protones = 11 23 Núcleo Na entonces este átomo Neutrones= 12 11 Corteza Electrones= 11 Actividad 3 Completen la siguiente tabla considerando que todos los datos corresponden a átomos neutros. Elemento Símbolo Z A P+ e- 6 n 6 31 15 24 28 30 49 115 83 77 35 126 192 80 35 12 12 Actividad 4. Explica los tres postulados básicos que constituyen el principio de construcción: a) Principio de mínima energía: _______________________________________________________ 5 __________________________________________________________________ __________________________________________________________________ __________________________________________________________________ __________________________________________________________________ ____________________________ b) Principio de exclusión de Pauli: ____________________________________________________ __________________________________________________________________ __________________________________________________________________ __________________________________________________________________ __________________________________________________________________ __________________________________________________________________ ______ c) Principio de máxima multiplicidad:__________________________________________________ __________________________________________________________________ __________________________________________________________________ __________________________________________________________________ __________________________________________________________________ ____________________________ Actividad 5 Determina la configuración electrónica global externa de los siguientes elementos: Element o Be K K1+ C Al Al3+ Ca Cl F Li S Configuración electrónica global externa
© Copyright 2026