Trabajo Práctico Nº - Aula Virtual FCEQyN
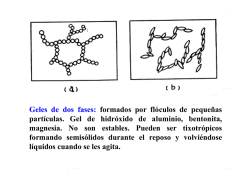
UNIVERSIDAD NACIONAL DE MISIONES Facultad de Ciencias Exactas Químicas y Naturales Ingeniería en Alimentos. Cátedra: Química y Bioquímica de los Alimentos Dr. Ing. Luis A. Brumovsky – Mgter. Bqca. Marta A. Horianski Trabajo Práctico Nº 4 - 2014 1 TRABAJO PRÁCTICO Nº 4 PROPIEDADES FUNCIONALES DE LAS PROTEÍNAS GELIFICACIÓN Objetivos ¬ Evaluar propiedades de interacción proteína-proteínas mediante el empleo de diferentes métodos. ¬ Determinar capacidad de gelificación de diversas proteínas. ¬ Caracterizar los geles obtenidos. Introducción La gelificación consiste en una agregación ordenada de proteínas con importantes cambios conformacionales. Es un proceso complejo que lleva consigo, en un primer paso, un desdoblamiento o desnaturalización de las proteínas, para después favorecer la interacción proteína-proteína que da origen a la estructura tridimensional ordenada en la que quedan retenidos el agua, los glóbulos de grasa, las sales y otras sustancias de bajo peso molecular. La gelificación es una propiedad funcional muy importante de algunas proteínas, se utiliza no solo para formar geles sólidos viscoelásticos, sino también para mejorar la absorción de agua, los efectos espesantes, la fijación de partículas (adhesión) y para estabilizar emulsiones y espumas. Son geles proteicos alimentos como: yogurt, queso, budín, salchicha, tofu, etc. Clasificación microestructural de geles proteicos Desde el punto de vista microestructural se pueden formar dos tipos de geles proteicos: - Tranrslúcidos - Alta retención de agua Condiciones de gelificación Se forman luego del enfriamiento (Gelatina) - Se forman durante el calentamiento (proteína de soja Caseína, Clara de huevo Microestructura Características 1. Redes por asociación física 2. Redes particuladas Geles agregados Geles ordenados Opacos Baja etención de agua Tranrslúcidos Alta retención de agua En la Figura 1 se observan la microestructura de los tipos de geles proteicos a) b) c) Figura 1. Microestructura de los geles proteicos. a) Asociación física, b) Ordenados, c) Agregados Obtención de geles proteicos Tratamiento térmico: Es el método más común para la gelificación de las proteínas. Hidrólisis enzimática moderada: Sin tratamiento térmico (micelas de caseína, clara de huevo, fibrina). 1 Trabajo Práctico Nº 4 - 2014 UNIVERSIDAD NACIONAL DE MISIONES Facultad de Ciencias Exactas Químicas y Naturales Ingeniería en Alimentos. Cátedra: Química y Bioquímica de los Alimentos Dr. Ing. Luis A. Brumovsky – Mgter. Bqca. Marta A. Horianski 2 Adición de iones Ca++ : Micelas de caseína y proteínas de soja. Tratamiento a altas presiones. Cambio de pH: Aunque en muchos casos puede obtenerse un coagulo que se separa del solvente. En los alimentos fermentados, el cambio de pH ocasionado por la formación de ácido láctico por las bacterias, produce la gelificación de la matriz proteica (salame, yogures). Mecanismo de gelificación de las proteínas globulares por tratamiento térmico La gelificación por calor se produce en varias etapas Figura 2. 1. Desnaturalización de la proteína por acción del calor 2. Interacción entre sí de las moléculas desnaturalizadas y formación de agregados. 3. Formación de una matríz primaria con propiedades viscoelásticas 4. Formación de una matríz de equilibrio, para ello se requiere tiempo y enfriamiento. Figura 2. Etapas de gelificación por calor de proteínas globulares La capacidad de formación de geles de las distintas proteínas y características tales como la rigidez, la textura, etc. de cada gel es muy variable y no todas las proteínas los producen en las mismas condiciones. La dureza del gel depende de la intensidad de las fuerzas (uniones hidrófobas, hidrófilas y covalentes) que constituyen dicha estructura y estas a su vez se ven afectadas por factores como: concentración de proteína, fuerza iónica, tipos de solutos, presencia de otros componentes en el medio, temperatura a la que es sometida y tiempo de gelificación, pH, grado de desnaturalización de la proteína, etc. Los geles de la carne son más estables cuando se inducen entre 60 y 70° C; sin embargo. a esta temperatura los de la soya son muy débiles e inestables y se consiguen mejor cuando la temperatura alcanza 90 o 100° C. Las mezclas a base de carne-soya que se usan para fabricar embutidos llegan a presentar algunos problemas de gelificación, pues en el proceso comercial se calientan a 70°C; sin embargo, con un tratamiento térmico adecuado que induzca la desnaturalización de las proteínas de soya se llega a mejorar sus propiedades gelificantes. 2 UNIVERSIDAD NACIONAL DE MISIONES Facultad de Ciencias Exactas Químicas y Naturales Ingeniería en Alimentos. Cátedra: Química y Bioquímica de los Alimentos Dr. Ing. Luis A. Brumovsky – Mgter. Bqca. Marta A. Horianski Trabajo Práctico Nº 4 - 2014 3 DESARROLLO PRÁCTICO Nº 4 PROPIEDADES FUNCIONALES DE LAS PROTEÍNAS GELIFICACIÓN Consignas - Determinar la capacidad de formar estructuras tipo gel en función de la temperatura y la concentración. Evaluar el efecto del pH sobre las características de los geles formados. Determinar la capacidad de retención de agua de los geles obtenidos mediante el método que emplea papel de filtro. Determinación de la capacidad de formar estructuras tipo gel · Efecto de la temperatura y la concentración: Se realiza a temperaturas próximas a la de desnaturalización de la proteína además para formar una red proteica autoestable se necesita una concentración proteica mínima conocida como concentración mínima de gelificación por debajo de la cual no es posible la obtención de geles. Materiales y métodos Muestra: - Gelatina - Proteína de soja, proteínas del suero láctico. Materiales: Tubos de ensayos Pipetas Probeta de 100 ml Tapones de goma - Mechero de bunsen - Baño María invertido Reactivos: - Agua destilada - Balanza Cronómetro Termómetro Heladera Baño termostatizado Equipos: Metodología Muestra: Gelatina (proteínas de colágeno modificadas) 1. Preparar 5 ml de distintas dispersiones de gelatina (0,5, 2 y 5% p/v) con agua destilada, previamente calentada a tres temperaturas diferentes (60, 80 y 100° C). 2. Mezclar vigorosamente evitando que se forme un aglomerado en el fondo del recipiente. 3. Colocarlas en tubos de ensayos, uno para cada concentración y temperatura. 4. Tapar herméticamente 5. Mantenerlas 1 hora a 4 °C. Muestra: Proteínas de soja o proteínas del suero láctico 1. Preparar 5 ml de dispersiones de proteínas en agua destilada al 5, 10 y 13 % P/V. 2. Colocar las dispersiones en tubos de ensayos y cerrarlos herméticamente. 3. Calentar los tubos, para inducir la gelificación de las proteínas de soja en un baño de agua a 60, 80 y 100° C durante 30 min. 4. Enfriar inmediatamente en un baño de agua a 15° C. 5. Mantener los geles 1 hora a 4° C. 3 Trabajo Práctico Nº 4 - 2014 UNIVERSIDAD NACIONAL DE MISIONES Facultad de Ciencias Exactas Químicas y Naturales Ingeniería en Alimentos. Cátedra: Química y Bioquímica de los Alimentos Dr. Ing. Luis A. Brumovsky – Mgter. Bqca. Marta A. Horianski 4 Posteriormente, para ambas ensayos 6. Vaciar cuidadosamente el contenido de los tubos 7. Observar si hubo formación de gel, y registrar las siguientes características: color, opacidad y textura. Sobre la base de los resultados obtenidos, determinar las condiciones temperatura/concentración que permita obtener geles de características determinadas. Para asegurar la completa gelificación se debería mantener los geles a 4º C durante 24 - 48 h. · Efecto del pH: El pH influye sobre las características de los geles formados. Materiales y métodos Muestra: - Yema de huevo. Materiales: Placas de Petri Vaso de precipitado Pipetas Probeta de 100 ml Tubos de ensayos Tapones de goma Cilindros de vidrio con tapones - Mechero de bunsen - Baño María invertido Reactivos: - Agua destilada NaCl al 0,5 % HCl 2N OHNa 2N - Cronómetro Medidor de pH Termómetro Heladera Baño termostatizado Equipos: Metodologia 1. 2. 3. 4. 5. Separar las claras de las yemas. Colocar las yemas en una caja de Petri y cortar las membranas que las recubren Colocar el contenido en un vaso de precipitado o tubo. Diluir las yemas 1:1 con NaCl 0.5%. Dividir en tres alícuotas y ajustar cada una a un pH diferente, 4, 7 y 11, empleando HCl o NaOH 2N. 6. Para obtener los geles colocar 10 ml de las dispersiones en tubos (cilindros de vidrio con tapones en los extremos) 7. Calentar 10 min a 95° C. 8. Enfriar inmediatamente en un baño de agua a 15° C. Para asegurar la completa gelificación es necesario mantener los geles a 4° C durante 24-48 h. En el trabajo experimental los geles se dejarán reposar 1 h a 4 °C en heladera. 9. Desplazar el gel con un émbolo para retirarlo del tubo. 10. Observar si hubo formación de gel, si hay líquido liberado, etc. Registrar las siguientes características: color, opacidad y textura. Sobre la base de los resultados obtenidos, relacionar las características de los geles con la condición pH utilizado. 4 Trabajo Práctico Nº 4 - 2014 UNIVERSIDAD NACIONAL DE MISIONES Facultad de Ciencias Exactas Químicas y Naturales Ingeniería en Alimentos. Cátedra: Química y Bioquímica de los Alimentos Dr. Ing. Luis A. Brumovsky – Mgter. Bqca. Marta A. Horianski 5 Una vez que destape el tubo donde obtuvo los geles de yema de huevo debe proceder con rapidez para determinar la capacidad de retención de agua. Capacidad de retención de agua de geles proteicos Se puede determinar mediante dos métodos por: - Papel de filtro. - Centrifugación · Determinación de la capacidad de retención de agua en papel de filtro Materiales y métodos Muestra: - Gel de yema de huevo Materiales: - Cuchillo Placas de Petri Regla Papel de filtro - Cronómetro Estufa Equipos: Metodología Trabajar con los geles obtenidos en el punto anterior. Una vez que destape el tubo donde obtuvo los geles de yema de huevo debe proceder con rapidez para determinar la capacidad de retención de agua. 1. Secar los papeles de filtro en estufa durante 10 minutos. 2. Desplazar el gel hacia fuera del tubo. 3. Cortar los geles en estudio en dos secciones transversales de 1 cm de espesor. 4. Depositar cada sección rápidamente en el centro del papel de filtro previamente secado. 5. Luego de tres minutos de contacto entre el gel y el papel de filtro marcar el halo formado. 6. Calcular el % de exudado como: E% = Donde: ( − ) 100 D3 = Diámetro del halo luego de tres minutos de contacto D0 = Diámetro interno del tubo. · Determinación de la capacidad de retención de agua por centrifugación Se utiliza un sistema de cilindro de acrílico, que contiene tres secciones A, B y C, con una membrana interna. Este se coloca con el gel en estudio en el interior de un tubo de centrífuga y se centrifuga determinando así la capacidad de retención de agua por centrifugación. Figura 3. Materiales y métodos Muestra: - Gel de yema de huevo. Materiales: - Cuchillo - Placas de Petri - Cilindro de acrílico con las tres secciones y membrana Equipos: - Centrífuga 5 Trabajo Práctico Nº 4 - 2014 UNIVERSIDAD NACIONAL DE MISIONES Facultad de Ciencias Exactas Químicas y Naturales Ingeniería en Alimentos. Cátedra: Química y Bioquímica de los Alimentos Dr. Ing. Luis A. Brumovsky – Mgter. Bqca. Marta A. Horianski 6 Metodología 1. Pese los cilindros A y B. 2. Corte una porción del gel de yema de huevo con un sacabocado y colóquela sobre la membrana 3. 4. 5. 6. del cilindro B. Vuelva a pesar los cilindros (A y B) con la muestra. Ubíquelos dentro del tubo de centrífuga colocando en primer lugar el cilindro C. Luego de centrifugar (ver condiciones) vuelva a pesar los cilindros (A y B) con el gel. Calcule la masa de agua perdida (diferencia en peso) en relación a la masa de gel y compare los resultados obtenidos trabajando en diferentes condiciones. A B C Figura 3. Cilindro con las secciones A, B, C y membrana. Referencias bibliográficas CHEFTEL J. C., CUQ J. L. Y LOIENT D. Proteínas alimentarias. Bioquímica. Propiedades funcionales. Valor nutritivo. Modificaciones químicas. Editorial Acribia. (1989). Zaragoza, España. FENNEMA, O. R., PARKIN, K. L. DAMORAN, S. Fennema química de los alimentos. 3a edición, Editorial CRC Press. Edición en la lengua española editorial Acribia S. A. (2008) España. GUÍA DE TRABAJOS PRÁCTICOS DE LABORATORIO. Cátedra de química de los alimentos. Licenciatura en ciencia y tecnología de alimentos. Facultad de Ciencias Exactas y Naturales – Universidad de Buenos Aires (2007). GUÍA DE TRABAJOS PRÁCTICOS: Propiedades funcionales. Cátedra de propiedades físicas y químicas de los alimentos ll. Facultad de Ciencias Exactas. UNLP. (2007). PILOSOF A. M. R. Y BARTHOLOMAI G. B. Caracterización funcional y estructural de proteínas. Editorial Eudeba. (2000). Bs. As. Argentina. SALFIELD J. R. (1977). Prácticas de ciencias de los alimentos. Editorial Acribia, Zaragoza, España. 6
© Copyright 2026