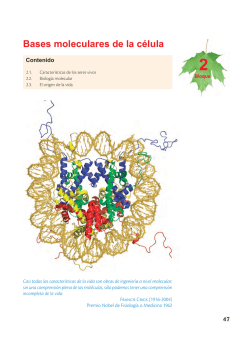
KARP_7a_c15_SENALIZACION_CELULAR
BIOLOGÍA CELULAR Y MOLECULAR Capítulo 15 Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Todos los derechos reservados. McGraw-Hill Interamericana Editores Señalización celular y transducción de señales: comunicación intercelular 15.1 Los elementos básicos de los sistemas de señalización celular 15.2 Estudio de los mensajeros extracelulares y sus receptores 15.3 Receptores unidos a proteína G y sus segundos mensajeros 15.4 Fosforilación de proteína tirosina como mecanismo para la transducción de señal 15.5 Función del calcio como mensajero intracelular 15.6 Convergencia, divergencia y comunicación cruzada entre diferentes vías de señalización 15.7 Función del óxido nítrico como mensajero intercelular 15.8 Apoptosis (muerte celular programada) PERSPECTIVA HUMANA: Trastornos relacionados con los receptores unidos a proteína G Vías de señalización y longevidad humana BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.1 Tipos de señalización intercelular autocrina (a), paracrina (b) y endocrina (c). BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.2 Revisión de las vías de señalización por las cuales las moléculas mensajeras extracelulares pueden inducir respuestas intracelulares. Se muestran dos tipos diferentes de vías de transducción de señal, una en la que se activa la vía de señalización mediante un segundo mensajero con capacidad de difusión y otra vía que se activa mediante el reclutamiento de proteínas a la membrana plasmática. La mayor parte de las vías de transducción de señales implica una combinación de estos mecanismos. También se debe señalar que las vías de señalización no siempre son trayectos lineales como los que se muestran aquí, sino que se ramifican y conectan para formar una compleja red. Los pasos se describen en el texto. BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.3 Vía de transducción de señal consistente en proteínas cinasas y proteínas fosfatasas cuyas acciones catalíticas cambian las conformaciones, y por lo tanto, las actividades de las proteínas que modifican. En el ejemplo que se muestra, la proteína cinasa 2 se activa por acción de la proteína cinasa 1. Una vez activada, la enzima 2 fosforila a una tercera enzima 3, lo que activa la misma. Después, la proteína cinasa 3 fosforila a un factor de transcripción, lo que aumenta su afinidad por un sitio en el DNA. La unión de un factor de transcripción con el DNA afecta la transcripción del gen en cuestión. Cada uno de estos pasos de activación de la vía se revierte con una fosfatasa. BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.4 Comparación de la frecuencia de fosforilación de tirosina en dos tipos de células de cáncer mamario. Los conjuntos del lado izquierdo indican la frecuencia de residuos fosfotirosínicos (pTyr en algunas proteínas) (señaladas en la mitad derecha de la figura) en líneas triplemente negativas del cáncer mamario. Tales células no expresan tres “signos” moleculares mayores de muchas células de cáncer mamario: receptores de estrógeno, de progesterona y del factor de crecimiento HER2. La frecuencia de residuos pTyr en células de cáncer mamario que expresan las tres proteínas “definitorias” se muestran en el conjunto de la derecha. La frecuencia de residuos pTyr de la proteína particular en una línea celular precisa indica la intensidad del polo rojo del cuadrado (consulte los pies en la parte inferior de la figura). A lo largo de la zona superior de la figura están los nombres de las líneas celulares estudiadas y se advierte que las células triplemente negativas tienen un grado mucho mayor de fosforilación de tirosina que las demás células cancerosas; ello pudiera depender de la pérdida de la actividad de una proteína tirosina fosfatasa particular (PTPN12) en muchas de las células propiamente negativas. (Con autorización de J. G. Albeck y J. S. Brugge, a partir de datos de Ting-Lei Gu, of Cell Signaling Technology, Cell 144:639, 2011. Reimpresa con autorización de Elsevier.) BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.5 La maquinaria unida a la membrana para la transducción de señales mediante un receptor con siete hélices transmembrana y una proteína G heterotrimérica. (a) Los receptores de este tipo, incluidos los que se unen con la adrenalina y el glucagón, contienen siete hélices que cruzan la membrana. Cuando se unen con su ligando, el receptor interactúa con una proteína G trimérica, la cual activa un efector, como la adenilil ciclasa. Como se indica en la figura, las subunidades α y γ de la proteína G están unidas con la membrana mediante grupos de lípidos que se incrustan en la bicapa lipídica. (Nota: muchos GPCR pueden activarse como complejos de dos o más moléculas receptoras.) BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.5 La maquinaria unida a la membrana para la transducción de señales mediante un receptor con siete hélices transmembrana y una proteína G heterotrimérica. (Continuación) (b) Un modelo que muestra la activación del GPCR rodopsina con base en estructuras cristalográficas de rayos X recientes. A la izquierda se muestra la rodopsina en su conformación inactiva (adaptada a la oscuridad), junto con una proteína G heterotrimérica no unida (llamada transducina). Cuando el cofactor retinal (mostrado en rojo en la molécula izquierda de rodopsina) absorbe un fotón, experimenta una reacción de isomerización (de su forma cis a la trans), lo que rompe un enlace iónico entre los residuos de la tercera y la sexta hélices transmembrana de la proteína. A su vez, este fenómeno produce un cambio en la conformación de la proteína que incluye movimiento hacia fuera de la sexta hélice transmembrana (flecha roja curva), lo cual expone un sitio de unión para la subunidad Gα de la proteína G. La molécula de rodopsina a la derecha se muestra en la conformación activa propuesta con una parte de la subunidad Gα (en rojo) unida con la cara citoplásmica del receptor. (b: tomada de Thue W. Schwartz y Wayne L. Hubell, Nature 455,473, 2008. Reimpresa con autoriczción de Macmillan Publishers Limited.) BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.6 El mecanismo de activación (o inhibición) mediado por receptor de los efectores mediante las proteínas G heterotriméricas. En el paso 1, el ligando se une con el receptor, lo que altera su conformación y aumenta su afinidad por la proteína G con la que se une. En el paso 2, la subunidad Gα libera su GDP, que se sustituye con GTP. En el paso 3, la subunidad Gα se separa del complejo Gβγ y se une con un efector (en este caso, adenilil ciclasa), lo que activa al efector. El dímero Gβγ también puede unirse con un efector (no se muestra), como un conducto iónico o una enzima. En el paso 4, la adenilil ciclasa activada produce cAMP. En el paso 5, la actividad de la GTP-asa de G_ hidroliza al GTP unido, lo que desactiva Gα. En el paso 6, Gα se relaciona de nueva cuenta con Gβγ, con lo que se reintegra la proteína G trimérica y el efector suspende su actividad. En el paso 7, el receptor ya se fosforiló por acción de una GRK y en el paso 8 el receptor fosforilado se unió con una molécula de arrestina, lo cual inhibe al receptor unido con ligando para que no active más proteínas G. Es probable que el receptor unido con la arrestina se capte por endocitosis. BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.7 Internalización de GPCR mediadas por arrestina. Los GPCR unidos a arrestina (paso 1) se internalizan cuando quedan atrapados en las depresiones recubiertas de clatrina que penetran en el citoplasma (paso 2). Como se señala en la sección 8.8, las esférulas recubiertas de clatrina son transformadas en vesículas con el mismo revestimiento que transportan su contenido, incluido en GPCR en los endosomas. Al estar en los endosomas, las arrestinas actúan como “andamiajes” para el ensamblado de complejos señalizadores, que incluyen los que activan la cascada de MAPK y el factor de transcripción ERK (paso 3). Otra posibilidad, es que los GPCR sean transportados a los lisosomas, sitio en que los receptores son degradados (paso 4) o devueltos a la membrana plasmática en un endosoma de reciclado (paso 5), sitio en que interactuarán con nuevos ligandos extracelulares (paso 6). (Con autorización de S.L. Ritter y R.A. Hall, Nature Reviews Mcb 10:820, 2009, Box 1B. Nature Reviews Molecular Cell Biology by Nature Publishing Group. Reproducida con autorización de Nature Publishing Group en el formato “Reutilizar en libro/ libro de texto” vía copyright Clearance Center.) BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Perspectiva Humana Figura 1 Representación bidimensional de un receptor transmembrana “compuesto” que muestra los sitios aproximados de varias mutaciones causantes de enfermedades humanas. La mayor parte de las mutaciones (números 1, 2, 5, 6, 7 y 8) produce estimulación constitutiva del efector, pero otras (3 y 4) bloquean la capacidad del receptor para estimular al efector. Las mutaciones en los sitios 1 y 2 se encuentran en el receptor para la MSH (hormona estimulante de los melanocitos); 3 en el receptor para ACTH (hormona adrenocorticotrópica); 4 en el receptor para vasopresina; 5 y 6 en el receptor para TSH (hormona estimulante de la tiroides); 7 en el receptor para LH (hormona luteinizante), y 8 en la rodopsina, el pigmento fotosensible de la retina. BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.8 Formación de cAMP en una célula viva como respuesta a la adición de una molécula mensajera extracelular. Esta serie de fotografías muestra una célula nerviosa sensitiva de la liebre marina Aplysia. La concentración de cAMP libre está indicada por colores: azul, amarillo y rojo representan concentraciones bajas, intermedias y elevadas, respectivamente. La imagen izquierda muestra el nivel intracelular de cAMP en la neurona no estimulada; las siguientes tres imágenes representan los efectos de la estimulación con el neurotransmisor serotonina (5-hidroxitriptamina) en los tiempos indicados. Observe que las concentraciones de cAMP caen alrededor de los 109 s a pesar de la presencia constante del neurotransmisor. (En este experimento, el nivel de cAMP se determinó de manera indirecta con la microinyección de una proteína cinasa dependiente de cAMP con marca fluorescente, con fluoresceína y rodamina en subunidades distintas. La transferencia de energía entre las subunidades (pág. 738) proporciona una medida de la concentración de cAMP.) (Reimpresa con autorización de Brian J. Backsai, et al., Science 260:223, 1993; © 1993 American Association for the Advancement of Science.) BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.9 Segundos mensajeros con base de fosfolípido. (a) Estructura de un fosfolípido generalizado (fig. 2.22). Los fosfolípidos están sometidos al ataque de cuatro tipos de fosfolipasas que dividen la molécula en los sitios indicados. De estas enzimas, la descripción se enfoca en la PLC, que divide el grupo cabeza fosforilado del diacilglicerol (fig. 15.10). (b) Modelo que muestra la interacción entre una porción de una molécula de enzima PLC que contiene un dominio PH que se une con el anillo de inositol fosforilado de un fosfoinosítido. Esta interacción sujeta a la enzima con la superficie interna de la membrana plasmática y puede alterar su actividad enzimática. (c) Micrografía con fluorescencia de una célula que se estimuló para moverse hacia un quimioatrayente (una sustancia que atrae a la célula). Esta célula se tiñó con un anticuerpo que se une de manera específica con el 3,4,5-trifosfato de PI (PIP3), el cual se observa en el margen principal de la célula migratoria (flechas). La barra representa 15 m. (b: tomada de James H. Hurley y Jay A. Grobler, Curr Opin Struct Biol 7:559, 1997; c: tomada de Paula Rickert et al., por cortesía de Henry R. Bourne, University of California, San Francisco, Trends Cell Biol 10:470, 2000. Ambas imágenes reimpresas con autorización de Elsevier.) BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.10 Generación de segundos mensajeros como resultado de la degradación inducida por ligando de los fosfoinosítidos (PI) en la bicapa lipídica. En los pasos 1 y 2 se agregan grupos fosfato mediante las cinasas de lípidos al fosfatidilinositol (PI) para formar PIP2. Cuando el receptor capta un estímulo, el receptor unido con ligando activa una proteína G heterotrimérica que tiene una subunidad G_q (paso 3) que activa a la enzima fosfolipasa C específica para PI (paso 4), la cual cataliza la reacción en la que PI(4, 5)P2 se divide en diacilglicerol (DAG) y 1,4,5-trifosfato de inositol (IP3) (paso 5). El DAG recluta la proteína cinasa PKC a la membrana y activa la enzima (paso 6). IP3 se difunde hacia el citosol (paso 7), donde se une con un receptor IP3 y un conducto del calcio en la membrana del retículo endoplásmico liso (SER) (paso 8). La unión de IP3 con su receptor produce la liberación de iones calcio hacia el citosol (paso 9). BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.11 Demostración experimental de los cambios en la concentración de calcio libre en respuesta a la estimulación hormonal. Una sola célula hepática se inyectó con acuorina, una proteína extraída de cierta medusa que produce luminiscencia cuando se une con iones de calcio. La intensidad de la luminiscencia es proporcional a la concentración de iones libres de calcio. La exposición de la célula a la vasopresina produce espigas controladas en la concentración de calcio libre a intervalos periódicos. Las concentraciones más altas de hormona no aumentan la altura (amplitud) de las espigas, sino la frecuencia. (Reimpresa con autorización de N.M. Woods, K.S. Cuthbertson y P.H. Cobbold. Nature 319:601, 1986; © 1986. Nature de Nature Publishing Group. Reproducida con autorización de Nature Publishing Group en formato “Reutilizar en libro/libro de texto” a través de Copyright Clearance Center.) BIOLOGÍA CELULAR Y MOLECULAR Figura 15.12 Reacciones que conducen al almacenamiento o movilización de glucosa. Las actividades de dos de las enzimas clave en estas reacciones, la glucógeno fosforilasa y la glucógeno sintasa, están bajo el control de hormonas que actúan mediante vías de transducción de señales. La glucógeno fosforilasa se activa como respuesta al glucagón y a la adrenalina, mientras que la glucógeno sintasa se activa como reacción a la insulina (pág. 646). Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.13 La formación de cAMP a partir de ATP catalizado por acción de la adenilil ciclasa, una proteína integral de la membrana que se forma con dos partes, cada una con seis hélices transmembrana (mostradas en dos dimensiones). El sitio activo de la enzima se localiza en la superficie interna de la membrana, en una hendidura situada entre dos dominios citoplásmicos similares. La degradación del cAMP (no se muestra) se realiza mediante una fosfodiesterasa, la cual convierte al nucleótido cíclico en un 5’ monofosfato. BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.14 Respuesta de un hepatocito al glucagón o la adrenalina. Los pasos de la respuesta a la estimulación hormonal que culmina en la movilización de glucosa se describen en el texto. Muchas de las fases de la cascada reactiva se acompañan de una amplificación impresionante de la señal. Los pasos que culminan en la amplificación están indicados por cúmulos de flechas azules. La activación de la transcripción por CREB se produce conjuntamente con el grupo usual de coactivadores (p. ej., p300 y CBP) y complejos modificadores de cromatina (no se incluyen). BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.15 Ilustración de la variedad de procesos que pueden afectarse por los cambios de la concentración de cAMP. Se cree que todos estos efectos están mediados por la activación de la misma enzima, la proteína cinasa A. En realidad, la misma hormona puede inducir reacciones muy diferentes en distintas células, incluso cuando se une con el mismo receptor. Por ejemplo, la adrenalina se une con un receptor similar adrenérgico β en las células hepáticas, células adiposas y en las de músculo liso del intestino, lo que induce la producción de cAMP en los tres tipos celulares. Sin embargo, las respuestas son muy distintas: en la célula hepática se degrada glucógeno, en la célula adiposa se degradan triacilgliceroles y las células de músculo liso se someten a relajación. Se sabe que además de la PKA, el cAMP interactúa con conductos iónicos, fosfodiesterasas y GEF (pág. 641). BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.16 Representación esquemática de los complejos de señalización AKAP que operan en diferentes compartimientos subcelulares. La AKAP en cada uno de estos complejos proteínicos se representa por medio de la barra púrpura. En cada caso, la AKAP forma un andamiaje que une una molécula de PKA con los sustratos potenciales y otras proteínas implicadas en la vía de señalización, incluidas fosfatasas (triángulos verdes) que pueden eliminar los grupos fosfatos agregados. Las AKAP mostradas aquí dirigen la PKA a varios compartimientos distintos, incluidos membrana plasmática, mitocondria, citoesqueleto, centrosoma y núcleo. (Reimpresa con autorización de W. Wong y J. D. Scott, Nature Reviews Mol. Cell Biol. 5:961, 2004; © copyright 2004. Nature Reviews Molecular Cell Biology by Nature Publishing Group. Reproducida con autorización de Nature Publishing Group en formato para reutilizar en libro/libro de texto a través de Copyright Clearance Center.) BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.17 Pasos en la activación de una proteína tirosina cinasa receptora (RTK). (a) Dimerización mediada por ligando. En el estado no activado, los receptores se encuentran en la membrana como monómeros. La unión de un ligando bivalente induce la dimerización directa del receptor y la inducción de su actividad cinasa, lo que hace que agregue grupos fosfato al dominio citoplásmico de la otra subunidad receptora. Los residuos recién formados de fosfotirosina del receptor, sirven como sitios de unión para las proteínas blanco que contienen dominios SH2 o PTB. Las proteínas blanco, se activan como resultado de su interacción con el receptor. (b) Dimerización mediada por el receptor. La secuencia de fenómenos es similar a la de la parte a, excepto porque la molécula de ligando es monovalente y, por consiguiente, una molécula de ligando se une con cada uno de los monómeros inactivos. La unión de cada ligando induce un cambio de conformación en el receptor que crea una interfase de dimerización (flechas rojas). Los monómeros unidos con el ligando interactúan mediante esta interfase para convertirse en un dímero activo. (Basada en un dibujo de J. Schlessinger y A. Ullrich, Neuron 9:384, 1992; con autorización de Cell Press. Neuron by Cell Press. Reproducida con autorización de Cell Press en el formato “Reutilizar en libro/libro de texto” vía Copyright Clearance Center.) BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.18 Interacción entre un dominio SH2 de una proteína y un péptido que contiene un residuo de fosfotirosina. El dominio SH2 de la proteína se muestra en una vista cortada con la superficie accesible representada por puntos rojos y la columna del polipéptido como un listón púrpura. El heptapéptido que contiene fosfotirosina (Pro-Asn-pTyr-Glu-Glu-Ile-Pro) se muestra como un modelo que llena el espacio, cuyas cadenas laterales se colorearon de verde y la columna de amarillo. El grupo fosfato se muestra en azul claro. Se advierte que el residuo de tirosina fosforilado y el residuo de isoleucina (+3) se proyectan en sacos sobre la superficie del dominio SH2, generando una estrecha interacción, pero sólo cuando el residuo de tirosina clave se fosforila. (Tomada de Gabriel Waksman et al., por cortesía de John Kuriyan. Cell 72:783, 1993; reimpresa con autorización de Elsevier.) BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.19 Diversas proteínas de señalización. Las células contienen muchas proteínas con dominios SH2 o PTB que se unen con residuos de tirosina fosforilada. (a) Las proteínas adaptadoras, como la Grb2, funcionan como un vínculo con otras proteínas. Como se muestra aquí, Grb2 puede servir como vínculo entre un factor de crecimiento RTK activado y Sos, un activador de una proteína corriente abajo llamada Ras. La función de Ras se describe más adelante. (b) la proteína de acoplamiento IRS contiene un dominio PTB que le permite unirse con el receptor activado. Una vez unidos, el receptor fosforila a los residuos de tirosina en la proteína de acoplamiento. Estos residuos fosforilados funcionan como sitios de unión para otras proteínas de señalización. (c) Ciertos factores de transcripción se unen con las RTK activadas, un fenómeno que conduce a la fosforilación y activación del factor de transcripción y su traslado al núcleo. Los miembros de la familia STAT de factores de transcripción se activan de esta manera. (d) una gran variedad de enzimas de señalización se activa después de unirse con una RTK activada. En el caso mostrado aquí, una fosfolipasa (PLCgamma), una lipasa (PI3K) y una proteína tirosina fosfatasa (Shp2) se unieron con sitios de fosfotirosina en el receptor. BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.20 Estructura terciaria de una proteína adaptadora, Grb2. Grb2 se forma con tres partes: dos dominios SH3 y uno SH2. Los dominios SH2 se unen con una proteína (p. ej., el receptor EGF activado) que contiene un motivo particular que incluye un residuo de fosfotirosina. Los dominios SH3 se une con una proteína (p. ej., Sos) que posee un motivo particular rico en residuos de prolina. Se han identificado docenas de proteínas que tienen estos dominios. Las interacciones que implican dominios SH3 y SH2 se muestran en las figuras 2-40 y 15-18, respectivamente. Otras proteínas adaptadoras incluyen Nck, Shc y Crk. (Reimpresa con autorización de Sébastien Maignan et al. Science 268:291, 1995; © 1995 American Association for the Advancement of Science. Cortesía de Arnaud Ducruix.) BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.21 Estructura de una proteína G y el ciclo de la proteína G. (a) Comparación de la estructura terciaria del estado activo unido con GTP (rojo) y el estado inactivo unido con GDP (verde) de la pequeña proteína G Ras. Se muestra un nucleótido de guanina unido en la forma de esferas y cilindros. Las diferencias de la conformación ocurren en dos regiones flexibles de la molécula que se conocen como interruptores I y II. La diferencia de la conformación mostrada aquí afecta la capacidad de la molécula para unirse con otras proteínas. (b) Ciclo de la proteína G. Las proteínas G se hallan en su estado inactivo cuando se les une una molécula de GDP. Si la proteína G inactiva interactúa con un inhibidor de disociación de nucleótido de guanina (GDI), se inhibe la liberación de GDP y la proteína permanece en el estado inactivo (paso 1a). Si la proteína G inactiva interactúa con un factor de intercambio de nucleótido de guanina (GEF, paso 1b), la proteína G intercambia su GDP por un GTP (paso 2), lo cual activa la proteína G para que pueda unirse con una proteína blanco corriente abajo (paso 3). La unión con la proteína G unida con GTP activa a la proteína blanco, la cual casi siempre es una enzima, como una proteína cinasa o una proteína fosfatasa. Esto tiene el efecto de transmitir la señal más allá sobre la vía de señalización. Las proteínas G poseen una actividad intrínseca de GTP-asa débil, que se estimula con la interacción con una proteína activadora de GTP-asa (GAP) (paso 4). El grado de estimulación de la GTP-asa por una GAP determina el tiempo que permanece activa una proteína G. Por consiguiente, la GAP sirve como un tipo de reloj que regula la duración de la respuesta (paso 5). Una vez que se hidroliza el GTP, el complejo se disocia y la proteína G inactiva está lista para iniciar un nuevo ciclo (paso 6). (a: tomada de Steven J. Gamblin y Stephen J. Smerdon, Struct 7:R200, 1999. Reimpresa con autorización de Elsevier.) BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.22 Los pasos de una cascada de cinasa de MAP generalizada. La unión de un factor de crecimiento con su receptor (paso 1) conduce a la autofosforilación de residuos de tirosina del receptor (paso 2) y el reclutamiento subsiguiente de proteínas Grb2Sos (paso 3). Este complejo provoca el intercambio GTP-GDP de Ras (paso 4), la cual recluta a la proteína Raf a la membrana, donde se fosforila y luego se activa (paso 5). En la vía mostrada en esta figura, Raf se fosforila y activa a otra cinasa llamada MEK (paso 6), la que a su vez se fosforila y activa a otra cinasa más llamada ERK (paso 7). Este esquema de fosforilación en tres pasos mostrado en los pasos 5 a 7 es característico de todas las cascadas de cinasas de MAP. Por su actividad de cinasa en secuencia, Raf se conoce como una MAPKKK (cinasa de cinasa de cinasa de MAP), MEK es una MAPKK (cinasa de cinasa de MAP) y ERK como una cinasa MAP. Las MAPKK son cinasas de doble especificidad, término que denota que pueden fosforilar residuos de tirosina, serina y treonina. Todas las MAPK tienen un tripéptido cerca de su sitio catalítico con la secuencia Thr- X-Tyr. MAPKK fosforila a MAPK en el residuo de treonina y el de tirosina de esta secuencia, con lo que se activa la enzima (paso 7). Una vez activada, la MAPK se traslada al núcleo, donde fosforila factores de transcripción (TF, paso 8), como Elk-1. La fosforilación de los factores de transcripción incrementa su afinidad por los sitios reguladores en el DNA (paso 9), lo que conduce a un aumento de la transcripción de genes específicos (p. ej., Fos y Jun) que intervienen en la respuesta de crecimiento. Uno de los genes cuya expresión se estimula codifica una fosfatasa MAPK (MKP-1, paso 10). Los miembros de la familia MKP pueden retirar grupos fosfato de los residuos de tirosina y treonina de MAPK (paso 11), lo cual desactiva la MAPK y detiene la actividad de señalización en la vía. (Tomada de H. Sun y N.K. Tonks, Trends Biochem Sci 19:484, 1994. Trends in biochemical sciences by International Union of Biochemistry, Reproducido con autorización de Elsevier Ltd. en el formato de “Reutilizar en libro/libro de texto” vía Copyright Clearance Center.) BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.23 Funciones de las proteínas de “andamiaje” en la mediación de dos vías de MAPK de la levadura. (a) La vía de MAPK que regula el apareamiento en estas células, es inducida por un factor de apareo que se une a un GPCR, que es Ste2, que culmina en la activación de Gβγ que se une a la proteína de andamiaje Ste5, la cual a su vez se une a las proteínas MAPKKK, MAPKK y MAPK de la vía; (b) vía de MAPK que regula la respuesta osmorreguladora de la levadura en célula expuesta a una concentración alta de sodio. El receptor activado (Sho1) se liga a la proteína de andamiaje Pbs2 en su dominio SH3. El MAPKKK Ste11 es compartido en estas dos vías, pero es reclutado en una u otra respuestas por su interacción con el andamiaje proteínico apropiado. Pbs2 de andamiaje no recluta MAPKK separado, pero posee su propia actividad enzimática gracias a MAPKK. (c) Cuando las células son modificadas genéticamente para expresar un andamiaje quimérico Ste5-Pbs2 reaccionan a un factor de apareo al mostrar la respuesta osmorreguladora. (Véase Science 332:680, 2011, para una revisión de proteínas de andamiaje y este experimento.) BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.24 Respuesta del receptor para insulina a la unión con ligando. (a) El receptor para insulina, mostrado aquí de forma esquemática en su estado inactivo, es un tetrámero que consiste en dos subunidades α y dos α. (b) En este modelo, la unión de una sola molécula de insulina con las subunidades β produce un cambio de conformación en las subunidades β, lo cual induce la actividad de tirosinas cinasas de las subunidades β. (c) Las subunidades β activadas fosforilan residuos de tirosina situados en el dominio citoplásmico del receptor, así como los residuos de tirosina en varios sustratos del receptor para insulina (IRS) que se describen más adelante. BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.25 Función del IRS de tirosina fosforilado en la activación de varias vías de señalización. (a) Representación esquemática de un polipéptido IRS. La porción del extremo N de la molécula contiene un dominio PH que le permite unirse con fosfoinosítidos de la membrana y un dominio PTB que posibilita unirse con un residuo específico de tirosina fosforilada (núm. 960) en el dominio citoplásmico de un receptor para insulina activado. Una vez unido con el receptor para insulina, pueden fosforilarse varios residuos de tirosina del IRS (indicados como Y). Estas tirosinas fosforiladas sirven como sitios de unión para otras proteínas, incluida una cinasa de lípidos (PI3K), una proteína adaptadora (Grb2) y una proteína tirosina fosfatasa (Shp2). (b) Se sabe que la fosforilación del IRS por el receptor de insulina activado activa las vías de PI3K y Ras, que se describen en el capítulo. Otras vías aún no bien definidas también las activan los IRS. (El IRS se representa como una molécula bidimensional extendida para los fines de la ilustración.) (c) La activación de PI3K conduce a la formación de fosfoinosítidos unidas con la membrana, incluido el PIP3. Una de las cinasas claves en muchas vías de señalización es PKB (AKT), que interactúa en la membrana plasmática con PIP3 mediante un dominio PH en la proteína. Esta interacción cambia la conformación de la molécula PKB, lo que la convierte en sustrato para otra cinasa unida con PIP3 (PDK1) que fosforila a PKB. El segundo fosfato que se muestra unido con PKB se agrega por efecto de una segunda cinasa, más probablemente mTOR. Una vez activada, PKB se disocia de la membrana plasmática y se mueve hacia el citosol y el núcleo. PKB es el principal componente de varias vías de señalización separadas que median la respuesta a la insulina. Estas vías realizan la translocación de transportadores de glucosa a la membrana plasmática, síntesis de glucógeno y síntesis de nuevas proteínas en la célula. BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.26 Regulación de la captación de glucosa en las células musculares y adiposas por efecto de la insulina. Los transportadores de glucosa se almacenan en las paredes de vesículas citoplásmicas que se forman por gemación de la membrana plasmática (endocitosis). Cuando el nivel de insulina aumenta, se transmite una señal por la vía IRS-PI3K-PKB, lo cual inicia la translocación de vesículas citoplásmicas a la periferia celular. Las vesículas se fusionan con la membrana plasmática (exocitosis), lo que lleva a los transportadores a la superficie celular, donde pueden mediar la captación de glucosa. No se muestra una segunda vía que lleva del receptor de insulina a la transposición de GLUT4 (véase Trends Biochem. Sci. 31:215, 2006). (Según D. Voet y J.G. Voet, Biochemistry, 2nd ed. © 1995 John Wiley & Sons, Inc. Reimpresa con autorización de John Wiley & Sons, Inc.) BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Perspectiva Humana Figura 1 Efectos de la restricción calórica en los macacos Rhesus. Fotografías: (a) un típico animal testigo de 27.6 años de vida (el promedio de vida) y (b) animal de igual edad sometido a una dieta con restricción calórica. (Los resultados contrastantes señalados en el estudio NIA se pueden ver en la publicación on line 30/8/2012 número de Nature). (Con autorización de J. Colman, et al., Science 325:201, 2009. AAAS cortesía de Ricki Colman, Wisconsin National Primate Research Center, University of Wisconsin.) BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.27 Demostración experimental de la liberación localizada de Ca2+ intracelular dentro de la dendrita de una neurona. El mecanismo de liberación de Ca2+ mediado por IP3 de las reservas intracelulares se describe en la página 630. En esta micrografía, que muestra una célula (neurona) de Purkinje de una complejidad enorme del cerebelo, se liberaron iones de calcio al ambiente local dentro de una pequeña porción del complejo “árbol de dendritas”. La liberación de calcio (mostrada en rojo) se indujo en la dendrita después de la producción local de IP3, la cual sigue a la activación repetitiva de una sinapsis cercana. Los sitios de liberación de iones Ca2+ se revelan por la fluorescencia de un indicador de calcio fluorescente que se cargó en la célula antes de la estimulación. (Tomada de Elizabeth A. Finch y George J. Augustine. Nature, vol. 396, portada del 24/12/1998; Reimpresa con autorización de Macmillan Publishers Limited.) BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.28 Liberación de calcio inducida por calcio, tal y como ocurre en las células, como el músculo cardiaco. La despolarización en el voltaje de la membrana causa la abertura de los conductos del calcio activados por voltaje en la membrana plasmática, lo que permite la entrada de una pequeña cantidad de Ca2+ (paso 1) al citosol. Los iones calcio se unen con los receptores de rianodina en la membrana del retículo endoplásmico liso (paso 2), lo que induce la liberación del calcio almacenado en el citosol (paso 3), que inicia la contracción de la célula. Luego, los iones calcio son retirados del citosol por acción de bombas de Ca2+ situadas en la membrana del SER (paso 4) y un sistema de transporte secundario de Na+/Ca2+ en la membrana plasmática (paso 5), lo que causa la relajación. Este ciclo se repite después de cada latido cardiaco. (Reimpresa con autorización de M. J. Berridge, Nature 361:317, 1993; Copyright 1993. Nature by Nature Publishing Group. Reimpresa con autorización de Nature Publishing Group en el formato “Reutilizar en libro/libro de texto” vía de Copyright Clearance Center.) BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.29 Oleada de calcio en un huevo de estrella de mar inducida por la fecundación con un espermatozoide. Se inyectó un pigmento fluorescente sensible al calcio en el huevo no fecundado, luego se fecundó y se tomaron fotografías a intervalos de 10 s. Se observa que el incremento de la concentración de calcio se extiende del punto de entrada del espermatozoide (flecha) a todo el huevo. El color azul se refiere a [Ca2+] libre baja, mientras que el color rojo a [Ca2+] libre alta. Una oleada similar de Ca2+ se produce en los huevos de los mamíferos mediante la formación de IP3 por acción de una fosfolipasa C que introduce el espermatozoide al huevo durante la fecundación. (Cortesía de Stephen A. Stricker.) BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.30 Un modelo para la entrada de calcio operada por reservas. Cuando la luz del ER contiene abundantes iones Ca2+, las proteínas STIM1 de la membrana del ER y las proteínas Ora1 de la membrana plasmática se localizan de manera difusa en sus membranas respectivas y el conducto de calcio Ora1 se cierra. Si las reservas del ER se agotan, un sistema de señalización opera entre las dos membranas, lo que hace que las dos proteínas se aglomeren dentro de sus respectivas membranas, muy próximas una de otra. La interacción aparente entre las dos proteínas de membrana conduce a la abertura del conducto Ora1 y la entrada de iones Ca2+ al citosol, desde donde pueden bombearse hacia la luz del retículo endoplásmico. BIOLOGÍA CELULAR Y MOLECULAR Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.31 Calmodulina. Diagrama de cinta de la calmodulina (CaM) con cuatro iones calcio unidos (esferas blancas). La unión de estos iones Ca2+ cambia la conformación de la calmodulina y deja expuesta la superficie hidrófoba que promueve la interacción de Ca2+-CaM con una gran cantidad de proteínas blanco. Todos los derechos reservados. McGraw-Hill Interamericana Editores (Cortesía de Michael Carson, University of Alabama en Birmingham.) BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.32 Modelo simplificado de la función del calcio en el cierre de la célula de guardia. (a) Fotografía de los estomas, cada uno flanqueado por un par de células de guardia. Los estomas se mantienen abiertos mientras la presión de turgencia se conserva alta dentro de las células de guardia, lo que hace que se abulten hacia fuera como se advierte aquí. (b) Uno de los factores que controla el tamaño de los poros es la hormona ácido abscísico (ABA). Cuando se elevan las concentraciones de ABA, se abren los conductos iónicos para calcio de la membrana plasmática, lo que permite la entrada de Ca2+ (paso 1) y ello desencadena la liberación de Ca2+ de las reservas internas (paso 2). La elevación posterior de la concentración intracelular de calcio cierra los conductos de entrada de K+ (paso 3a) y abre los conductos de salida del K+ (paso 3b). Estos movimientos iónicos producen una caída de la concentración interna de solutos y pérdida osmótica de agua (paso 4). (La fosforilación por proteínas cinasas también tiene una función importante en estos procesos.) (a, Jeremy Burgess/Photo Researchers.) BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.33 Ejemplos de convergencia, divergencia y comunicación cruzada entre varias vías de transducción de señales. Este dibujo muestra los esbozos de las vías de transducción de señales iniciadas por receptores que actúan mediante proteínas G heterotriméricas y proteína tirosina cinasa receptoras. Se observa que las dos convergen por la activación de diferentes isoformas de fosfolipasa C y ambas conducen a la producción de los mismos segundos mensajeros (IP3 y DAG). La activación de RTK por PDGF o EGF da lugar a la transmisión de señales por tres vías diferentes, un ejemplo de divergencia. La comunicación cruzada entre los dos tipos de vías la ilustran los iones de calcio, que se liberan del retículo endoplásmico liso por acción de IP3 y luego pueden actuar sobre varias proteínas, incluida la proteína cinasa C (PKC), cuya actividad también se estimula por DAG. (M.J. Berridge, reimpresa con autorización de Nature vol. 361, p. 315, 1993. © 1993. Nature by Nature Publishing Group. Reproducida con autorización de Nature Publishing Group en el formato de “Reutilizar en libro/libro de texto” vía Copyright Clearance Center.) BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.34 Las señales transmitidas de un receptor unido con proteína G, una integrina y una tirosina cinasa receptora convergen en Ras y luego se transmiten a lo largo de la cascada de cinasa de MAP. BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.35 Un ejemplo de comunicación cruzada entre dos vías principales de señalización. El AMP cíclico actúa en algunas células mediante la cinasa PKA dependiente de cAMP para bloquear la transmisión de señales de Ras a Raf, la cual inhibe la activación de la cascada de cinasa de MAP. Además, la PKA y las cinasas de la cascada de cinasa de MAP fosforilan al factor de transcripción CREB en el mismo residuo de serina, lo que activa al factor de transcripción y permite que se una con sitios específicos del DNA. BIOLOGÍA CELULAR Y MOLECULAR Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.36 Una vía de transducción de señal que opera mediante el NO y el GMP cíclico y produce dilatación de los vasos sanguíneos. Los pasos ilustrados en la figura se describen en el texto. Todos los derechos reservados. McGraw-Hill Interamericana Editores (Tomada de R.G. Knowles y S. Moncada, Trends Biochem Sci 17:401, 1992. Trends in biochemical sciences de International Union of Biochemistry. Reproducido con autorización de Elsevier Ltd. en el formato “Reutilizar en libro/libro de texto” vía Copyright Clearance Center.) BIOLOGÍA CELULAR Y MOLECULAR Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Todos los derechos reservados. McGraw-Hill Interamericana Editores Figura 15.37 Comparación de una célula normal y células apoptóticas. (a,b) Micrografías electrónicas de barrido de una célula normal (a) y una célula apoptótica (b) de un hibridoma de linfocitos T. La célula que se somete a apoptosis tiene muchas vesículas superficiales que se desprenden de la célula. La barra equivale a 4 m. (c) Micrografía electrónica de transmisión de una célula apoptótica tratada con un inhibidor que detiene la apoptosis en la etapa de vesículas de membrana. (a y b: tomadas de S. J. Martin et al. Trends Biochem Sci 19:28, 1994. Reimpresa con autorización de Elsevier; c, cortesía de Nicola J. McCarthy.) BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.38 La apoptosis “modela” la estructura de los dedos de mamíferos. Tres etapas del proceso en un embrión de ratón. En el ratón particular, llamado MacBlue, todo los macrófagos embrionarios expresan la proteína fluorescente cian. Los macrófagos fluorescentes han infiltrado las regiones de la almohadilla de la pata en que se produjo la apoptosis y han “despejado” el espacio interdigital. (Con autorización de David A. Hume, Nature Immunol. 9:13, 2008; © 2008, reimpresa con autorización de Macmillan Publishers Limited.) BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.39 Modelo simplificado de la vía extrínseca (mediada por receptor) de la apoptosis. Cuando TNF se une con un receptor para TNF (TNFR1), el receptor activado se une con dos proteínas adaptadoras citoplásmicas diferentes (TRADD y FADD) y a la procaspasa 8 para formar un complejo multiproteínico en la superficie interna de la membrana plasmática. Los dominios citoplásmicos del receptor TNF, FADD y TRADD interactúan entre sí mediante regiones homólogas llamadas dominios de muerte que se encuentran en cada proteína (indicados como cuadros verdes). La procaspasa 8 y FADD interactúan mediante regiones homólogas llamadas dominios efectores de muerte (indicadas como cuadros cafés). Una vez ensambladas en el complejo, las dos moléculas de procaspasa se dividen una a la otra para generar una molécula activa de caspasa 8 que contiene cuatro segmentos polipeptídicos. La caspasa 8 es un complejo iniciador que divide a las caspasas corriente abajo (ejecutoras) que perpetran la sentencia de muerte. Puede notarse que la interacción entre TNF y TNFR1 también activa otras vías de señalización, una de las cuales conduce a la supervivencia celular en lugar de la autodestrucción (pág. 660). BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.40 Vía intrínseca (mediada por mitocondrias) de la apoptosis. Varios tipos de estrés celulares hacen que los miembros proapoptóticos de la familia de proteínas Bcl-2 (Bax o Bak) se oligomericen dentro de la membrana mitocondrial externa, y formen conductos que faciliten la liberación de moléculas de citocromo c desde el espacio intermembrana. En el citosol las moléculas del citocromo c forman un complejo con múltiples subunidades con una proteína citosólica llamada Apaf-1 y moléculas de procaspasas9; estas últimas al parecer son activadas hasta alcanzar su capacidad proteolítica plena como consecuencia de cambios en la conformación inducidos por la asociación con Apaf-1. Las moléculas de caspasa-9 desdoblan y activan las caspasas “de ejecución” que llevan a cabo la respuesta apoptótica. En algunas células la vía intrínseca puede ser desencadenada (como en los hepatocitos) por señales extracelulares; esta situación ocurre conforme la caspasa iniciadora de la vía extrínseca, la número 8 “separa” a una proteína BH3 exclusivamente llamada Bid, y genera un fragmento proteínico (tBid) que se une a Bax e induce la inserción de Bax en OMM y libera el citocromo c, de la mitocondria. BIOLOGÍA CELULAR Y MOLECULAR Todos los derechos reservados. McGraw-Hill Interamericana Editores Capítulo 15. Señalización celular y transducción de señales: comunicación intercelular Figura 15.41 La eliminación de las células apoptóticas se lleva a cabo por fagocitosis. Esta micrografía electrónica muestra el “cadáver” de una célula apoptótica dentro del citoplasma de un fagocito. Observe la naturaleza compacta de la célula englobada y el estado denso de su cromatina. (Reimpresa con autorización de Peter M. Henson, Donna L. Bratton y Valerie A. Fadok, Curr Biol 11:R796, 2001, Fig. 1a, Copyright 2001, con autorización de Elsevier.)
© Copyright 2026