INCUBACIÓN Y SU EFECTO EN EL DESEMPEÑO DEL
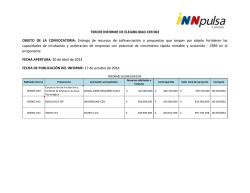
INCUBACIÓN Y SU EFECTO EN EL DESEMPEÑO DEL POLLITO EN LA PRIMERA SEMANA DE VIDA EDGAR O. OVIEDO-RONDÓN MVZ, PhD, Dip ACPV Prestage Departament of Poultry Science Universidad Estatal de Carolina del Norte, Raleigh, NC, 27606 [email protected] Introducción El título escogido para esta conferencia enfatiza los efectos de la incubación durante la primera semana de vida, pero en realidad la mayoría de los efectos de las condiciones en las que se desarrolle el embrión, afectan la salud y el desempeño del pollo por el resto de la vida post-eclosión e inclusive puede afectar algunas características de la canal al momento del sacrificio. Varios problemas de salud que se tratan de solucionar en las granjas con medidas de bioseguridad, tratamientos farmacológicos, planes vacunales y mayores inversiones en nutrientes en las dietas o en el agua, realmente tienen su origen y en gran parte solución al mejorar las condiciones de incubación. La incubación es un período en el que se desarrollan y maduran todos los órganos y sistemas fisiológicos que regulan el metabolismo y crecimiento como el sistema hormonal, al igual que el sistema respiratorio, y el inmunitario. El número de células de muchos tejidos como los músculos queda predeterminado antes de la eclosión y solo 1 sufren hiperplasia durante la vida post-eclosión. La muerte de algunas de estas células durante la última fase de incubación por hipoxia, falta de nutrientes a nivel tisular, cambios de pH, y estrés oxidativo, no se recupera en la vida adulta y están relacionados con los problemas de ascitis, muerte súbita, problemas de columna vertebral, problemas de emplume, pododermatitis y problemas óseos o de locomoción. Inclusive el desarrollo de la inmunidad en general puede afectarse puesto que incubaciones desuniformes causan ventanas de nacimiento muy prolongadas con pollitos que pueden demorar desde la eclosión hasta llegar a la granja más de 48 horas sin contacto con alimento o agua en el intestino. Efectos de la incubación en el desarrollo del embrión y desempeño del pollito En los últimos años he escrito varias revisiones (Oviedo-Rondón, 2008; Wineland y Oviedo-Rondón, 2009; Oviedo-Rondón y Wineland, 2011; Oviedo-Rondón, 2012a, b; Oviedo-Rondón, 2013, 2014a, b, c) sobre este tema, incluyendo parte de nuestros resultados de investigación sobre los efectos que las condiciones de incubación tienen en el desarrollo de los embriones y como los afecta en la vida post-eclosión. En los proyectos de investigación que conducimos principalmente estudiamos los efectos de perfiles de temperatura en los cuales no se obtiene la temperatura adecuada de la cáscara (37.8oC, 100oF) durante los primeros 3 días de incubación y existen temperaturas de la cáscara superiores a 38.5oC (101.3oF) durante los últimos 3 días de incubación. Estas condiciones se dan frecuentemente cuando no se precalienta los huevos antes de entrar a la máquina, se utilizan máquinas con múltiples cargas, y principalmente se mantiene una temperatura constante de nacedora entre 98.0oF y 97.5oF hasta la eclosión. Es decir estas condiciones son todavía muy frecuentes en condiciones comerciales. Este tratamiento de incubación subóptima generalmente lo comparamos con temperaturas de incubación en los que mantenemos la temperatura de la cáscara de los huevos cercana a 100oF durante los 21 días de incubación o comparamos también 2 con casos en donde solo se mantiene la temperatura de la nacedora constante y los huevos se sobrecalientan durante este período. En todas las 12 ocasiones en donde hemos evaluado estos efectos hemos observado reducciones en el desempeño de las aves independientemente de la línea genética o de tratamientos realizados en las reproductoras o después en la granja. El estrés que algunos embriones pueden estar expuestos durante la incubación se refleja en el tamaño del embrión, la organogénesis, el desarrollo fisiológico, la capacidad de eclosión y lógicamente se refleja en el desempeño del pollito (Decuypere y Michels, 1992; Yalçin y Siegel, 2003; Tazawa et al., 2004; Oviedo- Rondón et al., 2009; Molenaar et al., 2011). A manera de ejemplos en las Tablas 1 y 2 se presentan resultados de ganancia de peso, consumo de alimento y conversión alimenticia experimentos recientes con pollos Cobb. En los dos experimentos se evidencia el efecto deletéreo de los perfiles de temperatura subóptimos en el desempeño de los pollos durante las dos primeras semanas de vida y este efecto continua siendo significativo hasta casi el final del ciclo productivo. Tabla 1. Efecto de dos perfiles de temperatura durante la incubación en el desempeño de pollos de engorde Cobb 500 durante las dos primeras semanas de vida. Experimento 1. Perfil de temperatura durante incubación o Ganancia de peso 1-14 dias, g Hembras Machos 1 a Optima (100 F temp. cáscara) 2 Baja (primeros 3d)- Alta (3 d final) Error estándar a 453 b 429 4 474 b 461 7 Consumo de alimento, g Mixtos a a 459 b 435 6 583 b 559 6 Conversión alimenticia, g:g a 1.27 b 1.30 0.01 Fuente de variación -------------------------- Valores de probabilidad ----------------------Perfil de temperatura durante incubación <0.001 0.033 <0.001 <0.001 <0.001 1 2 o o Temperatura adecuada de la cáscara (37.8 C, 100 F) durante los 21 días de incubación. o o Temperatura de la cáscara baja (37.4 C, 99.5 F) durante los primeros 3 días de incubación y o o temperaturas de la cáscara superiores a 38.5 C (101.3 F) durante los últimos 3 días de incubación o o obtenidas al mantener la temperatura de la nacedora constante entre 98.0 F y 97.5 F. 3 Tabla 2. Efecto de tres perfiles de temperatura durante la incubación en el desempeño de pollos de engorde Cobb 500 durante las dos primeras semanas de vida. Experimento 2. Perfil de temperature durante incubación o Ganancia de peso 1-14 dias, g Hembras Machos Mixtos 1 ab Optima (100 F temp. cascara) 2 Optima – Alta (3 d final) 3 Baja (primeros 3d)- Alta (3 d final) Error estándar a 458 a 464 b 452 2 ab 464 a 465 b 451 4 459 a 463 b 451 3 Consumo de alimento, g Conversión alimenticia, g:g 576 584 574 6 1.13 1.14 1.14 0.01 Fuente de variación -------------------------- Valores de probabilidad ----------------------Perfil de temperatura durante incubación 0.0360 0.0170 0.0144 0.1818 0.2706 1 Temperatura adecuada de la cáscara (37.8 C, 100 F) durante los 21 días de incubación. o o 2 Temperatura adecuada de la cáscara (37.8 C, 100 F) durante 18 días de incubación y temperaturas de o o o o la cáscara superiores a 38.5 C (101.3 F) durante los últimos 3 días de incubación obtenidas al mantener o o la temperatura de la nacedora constante entre 98.0 F y 97.5 F. 3 o o Temperatura de la cáscara baja (37.4 C, 99.5 F) durante los primeros 3 días de incubación y o o temperaturas de la cáscara superiores a 38.5 C (101.3 F) durante los últimos 3 días de incubación o o obtenidas al mantener la temperatura de la nacedora constante entre 98.0 F y 97.5 F. Efectos de la incubación en la salud de los pollitos Las condiciones de incubación no solo afectan el desempeño. La salud de las aves también es afectada. En los últimos dos años hemos estado evaluando los efectos de perfiles de temperaturas de incubación sobre la incidiencia de pododermatitis y espondilolistesis. En cuanto a pododermatitis, De Jong et al. (2012) observaron que las condiciones de incubación tuvieron un efecto sobre la incidencia de pododermatitis. A pesar de que no se observó ninguna tendencia clara en pododermatitis entre las incubadoras, las diferencias informadas por De Jong et al. (2012) demostraron claramente la existencia de factores desconocidos que influyen en la incidencia de esta condición. 4 Swayer et al. (1984) reportaron que la morfogénesis de la piel, plumas, espuelas, escamas reticulares y escuteiformes se ven afectados por la interacción epidermis dermis durante el desarrollo embrionario. En consecuencia, cualquier parámetro de incubación que afecta el desarrollo del embrión puede afectar a la piel y sus apéndices. En un experimento realizado por Yalçin et al. (2008), se reportaron temperaturas elevadas (38,5°C) entre el 10 y 18 días de incubación para aumentar peso vivo al nacimiento pero afectaron negativamente el corazón y el hígado. Un hallazgo interesante observado es que las altas temperaturas de incubación tuvieron un efecto negativo en el desarrollo del pico a los 18 días de incubación. A pesar de que no se observaron diferencias entre la incubación óptima y tratamientos de altas temperaturas al nacimiento, las condiciones de estrés durante la incubación pueden tener un efecto en el desarrollo del tejido queratinoso. Concomitantemente con los efectos en la estructura y la composición corporal, también se reportan cambios en las regulaciones hormonales y metabólicas (Moraes et al., 2004; Yahav et al., 2004; Piestun et al., 2009). Piestun et al. (2009) observaron que las temperaturas de incubación altas (39,5oC) entre los días 7 y 16 de la incubación redujo la concentración plasmática de T3. Los niveles de hormonas de estrés también se aumentan cuando los huevos fueron expuestos a temperaturas elevadas (Iqbal et al., 1990; Moraes et al., 2004). Por otra parte, varios autores han demostrado un efecto negativo de la cortisona y la hidrocortisona en la morfogénesis escamas de la piel en pollos (Moscona y Karnofsky, 1960; Stuart et al., 1972; Fisher et al., 1984). Fisher et al. (1984) demostraron que todos los tipos de escamas de la piel se suprimieron cuando los embriones fueron expuestos a dosis de 40 mg de hidrocortisona a los 10 días de incubación. Además, las escamas reticuladas fueron específicamente ausentes en la parte más ventral de la almohadilla de la pata cuando los embriones fueron expuestos a altas dosis de hidrocortisona (Fisher et al., 1984). Estas alteraciones de la piel causadas por estrés durante la incubación pueden afectar la susceptibilidad a problemas de dermatitis. 5 Otro parámetro que debe ser considerada durante la incubación es condiciones de hipoxia. Varios investigadores han argumentado que la disponibilidad de oxígeno afecta el desarrollo de órganos del embrión (McCutcheon et al., 1982; Stock et al., 1983). Dzialowski et al. (2002) encontraron que los embriones expuestos a la hipoxia después del dia 12 de incubación tuvieron picos más cortos al ser medidos el 18avo día de incubación. Esto demuestra que el desarrollo de los tejidos queratinosos también se ven afectados por este parámetro de incubación. Teniendo en cuenta las conclusiones de De Jong et al. (2012) y las otras investigaciones antes mencionados fue posible deducir que el desarrollo de la piel de la almohadilla plantar pueden ser afectadas por las condiciones de incubación y deben ser consideradas como posibles factores predisponentes para la pododermatitis. La piel de la almohadilla plantar de las aves de corral se considera una estructura especializada tipo epidérmica que protege a las aves contra agentes mecánicos y químicos presentes en el medio ambiente (Michel, 1992). escamas en las patas de las aves (Sawyer y Knapp, 2003). Existen dos tipos de La parte dorsal del metatarso y dedos de los pies están cubiertos con escamas escuteliformes mientras que la superficie de la planta de los pies está cubierto de escamas reticulares (Prin et al., 2004). Las escamas están dispuestas en un patrón que no se solapan y tienen una estructura simétrica papilar (Prin et al., 2004). Histomorfológicamente, estas papilas tienen tres capas principales: el estrato córneo, la epidermis y la dermis (Bacha Jr. y Bacha, 2000). El desarrollo de la piel comienza en la etapa temprana del desarrollo embrionario, y para el final del noveno día de incubación, la parte anterior de la pata del embrión de pollo se cubre con una epidermis de dos capas (Sawyer, 1972; Bellairs y Osmond, 2005). La formación de escamas se inicia alrededor del 12o día de incubación y se completa al dia 16 (Sawyer 1972; Gonzales y Cesario, 2003; Bellairs y Osmond, 2005). Durante este período cada escama se incrementa, queratiniza, y los vasos sanguíneos aparecen en las papilas (Bellairs y Osmond, 2005). En la Universidad Estatal de Carolina del Norte realizamos cuatro experimentos para evaluar los efectos de las temperaturas de incubación sobre el desarrollo de la piel de 6 la almohadilla plantar y la incidencia de pododermatitis en pollos y patos. En todos los experimentos se evaluaron dos perfiles de temperatura de incubación en combinación con otros factores utilizando arreglos factoriales. Un tratamiento fue diseñado para mantener la temperatura de la cáscara cerca del óptimo (37.8oC, 100oF) y el segundo tratamiento tuvo temperaturas de cáscara de huevo similares a los observados en máquinas de carga múltiple. Este segundo perfil tuvo bajas temperaturas (36,9oC) de la cáscara durante los primeros 3 días, y 38,0oC hasta los últimos 3 días cuando los huevos fueron sometidos a elevadas temperaturas (38,9oC). En patos, los perfiles de temperatura cambiaron después de 12 días, y la conductancia de la cáscara de los huevos se redujo por inmersión de huevos en cera a los 14 días de incubación. En la incubación, se seleccionaron los pollitos o patitos de cada tratamiento y las almohadillas de las patas fueron muestreadas para el análisis histológico. Los patos se criaron hasta los 36 días y los pollos ya sea hasta 21 o 42 días de edad. Al final de cada experimento se evaluó la incidencia de pododermatitis. Los resultados indicaron que los perfiles de temperatura de incubación y la conductancia de la cáscara afectaron el desarrollo de la piel de la almohadilla plantar. La incubación subóptima aumenta la susceptibilidad a pododermatitis a medida que la humedad de la cama aumenta (Figura 1). Figura 1. Efecto de la temperatura de incubación en los escores de pododermatitis de pollos de engorde o Cobb 500 a los 28 días de edad. Dos tratamientos fueron evaluados temperatura optima de 38,0± 0.3 C o o (Standard) o baja (36,9 C) durante los primeros 3 días y elevada (38,9 C) durantes los últimos 3 días (low – high). La temperatura elevada de las cáscaras en nacedoras se obtuvo al mantener la o temperatura de la nacedora constante at 98,0-97.5 C. 7 Este efecto de la mala incubación en aumentar la susceptibilidad a la pododermatitis fue también explicado en otro experimento en donde evaluamos la expresión génica del interferon-γ y de varias interleucinas en la piel del cojinete plantar de pollitos provenientes de huevos incubados bajo tres perfiles de incubación. Estas moléculas promueven la inflamación inespecífica, migración de macrófagos y linfocitos. Otros investigadores han encontrado que la expresión génica de estas linfocinas se aumenta bastante en presencia de cama humeda. En este experimento utilizamos cama con humedad no mayor a 25%, pero teníamos cama nueva o usada. Parte de los resultados pueden observarse en la Figura 2. La expresión génica del interferon-γ y IL1β a los 4 días de edad estaba significativamente aumentada en pollitos, especialmente en las hembras, provenientes de huevos incubados bajo perfiles de alta temperatura en los últimos 3 dias de la incubación. Estos resultados están relacionados al mismo estrés inmunológico o inmunosupresión observada por Oznurlu et al. (2010) en pollitos de una semana provenientes de nacedoras con altas temperaturas (Tabla 3). Figura 2. Efecto de la temperatura de incubación (Standard, StdHigh or LowHigh) y el estado de la cama (nueva o usada) sobre la expresión de los genes de interferon-γ y IL-1β sobre la pododermatitis a los 4 días de vida. o Tabla 3. Efecto de temperaturas de la cáscara de 39 a 40 C durante los últimos 4 días de incubación en la inmunidad celular después de la eclosión. Porcentaje de linfocitos Relación H/L Edad del pollo (Media ± Error estándard) (Media ± Error estándard) Elevada Temp. Nacedora Control Eclosión 35·8 ± 4·2 a 30·2 ± 1·92 2 días 55·2 ± 9·6 a 42·0 ± 6·0 7 días 60·4 ± 4·6 a 53·4 ± 7·4 b Elevada Temp Nacedora Control 0·9 ± 0·2 b 1·5 ± 0·2 a b 0·6 ± 0·1 b 0·8 ± 0·1 a a 0·3 ± 0·1 b 0·6 ± 0·2 a Fuente: Oznurlu et al., 2010. BPSJ. 8 Este efecto negativo de la incubación subóptima sobre la inmunidad celular es aumentado todavía más cuando se generan ventanas de nacimiento muy prolongadas. Cuando alguna proporción de pollitos nace 40 horas o más antes de la extracción de las bandejas de las máquinas. Una proporción considerable de pollitos va a demorar mas de 48 horas para estar en contacto con alimento y comida. Estos ayunos prolongados post-nacimiento generan problemas con el desarrollo de la inmunidad del tracto gastroinstestinal como es observado en las Figuras 3 y 4. Figura 3. Efecto del ayuno (○) después de la eclosión por 48 horas en el desarrollo de la colonizacion de linfocitos en la bolsa de Fabricio durante las primeras dos semanas de vida, comparado con pollitos que tuvieron acceso a alimento y agua (●) (Bar-Shira et al., 2005). En un experimento realizado por el grupo de Bar-Shira et al. (2005) se observó que pollitos que pasaban 49 horas sin acceso a alimento y agua demoraban el número de células que colonizaban la bursa de fabricio en las dos semanas siguientes. Y el mismo ayuno, también causa una demora en la respuesta de anticuerpos a antígenos no específicos de los pollitos con ayuno hasta por dos semanas especialmente en el colon. Estas dos primeras semanas es cuando el ave debe reconocer los antígenos y las primeras vacunaciones son utilizadas. Si tenemos aves con estos problemas que vienen por problemas de incubación desuniforme, muy probablemente no vamos a tener una respuesta inmune uniforme y algunos patógenos como Salmonella se pueden establecer en el colon y ciego. Por esto, es muy importante mejorar la incubación especialmente buscando uniformidad. 9 En cuanto a espondilolistesis enterococcica hemos realizado experimentos para evaluar el efecto de incubación en el desarrollo de la ostechondritis dissecans que es el daño de los cartílagos de la columna vertebral entre la torácicas libres T5 y T6 que puede predisponer a los pollos a que una infección por Enteroccocus cecorum prolifere en esta área y se genere la lesión que paraliza al ave. En esta enfermedad se observan síntomas clínicos de parálisis entre la 4 y 6 semana de vida, pero la lesión inicial de la columna puede observarse por histopatología desde la primera semana de vida y la infección desde la segunda semana de vida. La lesión de ostechondritis dissecans esta correlacionada (r= 0.65) con la infección por Enteroccocus cecorum. En nuestros estudios hemos encontrado que esta lesión es aumentada por la mala incubación y esta levemente correlacionada con un aumento de la asimetría en la longitud de los huesos de las patas del animal. Es decir la incubación no adecuada por baja temperatura en la incubadora los primeros 3 días o alta temperatura en la nacedora principalmente causa que el ave no tenga los huesos de las patas simétricas y para mantener el centro de gravedad el animal genera movimientos de locomoción diferentes al normal que fuerzan a movimientos de la columna afectando el área de vertebras libres y generando el roce de estos cartílagos. El rozamiento causa la ostechondritis dissecans y después el Enteroccocus cecorum o cualquier otra bacteria con capacidad colagenolítica coloniza esta área en proceso de necrosis. 10 Figura 4. Efecto del ayuno (○) después de la eclosión por 48 horas en la respuesta de anticuerpos contra antígenos no específicos en el duodeno, yeyuno y colon durante las primeras dos semanas de vida, comparado con pollitos que tuvieron acceso a alimento y agua (●) (Bar-Shira et al., 2005). Conclusiones Las condiciones de temperatura y ventilación especialmente durante la fase inicial y final de la incubación tienen efectos permanentes en el desarrollo del embrión que afectan todo su crecimiento post-eclosión. Estos efectos pueden ser observados en la salud, bienestar animal, crecimiento, y desempeño de los lotes de pollos de engorde en la primera semana de vida y durante toda la vida del animal e inclusive en la calidad de la canal al sacrificio. Referencias Bar-Shira, E., D. Sklan, and A. Friedman. 2005. Impaired immune responses in broiler hatchling hindgut following delayed access to feed. Vet. Immunol. Immunopathol. 105:33– 45. Decuypere, E., and H. Michels. 1992. Incubation temperature as a management tool: A review.World’s Poult. Sci. J. 48:28–38. Molenaar, R., R. Hulet, R. Meijerhof, C.M. Maatjens, B. Kemp y H. van den Brand. 2011. Poult. Sci. 90:624-632. Oviedo Rondón, E.O. 2008. Industria Avícola. Watt Publishing, Julio, 55 (7): 14-16 Oviedo Rondón, E.O. 2012a. Manejo da incubação para melhorar performance, saúde e qualidade em frangos de corte. Anais da Reunião Brasil Sul de Avicultura, Chapecó, SC., Brazil. Abril, 2012. Oviedo Rondón, E.O. 2013. Breeder nutrition and effects on incubation and quality of the chick. In CD Proceedings of International Symposium of AMEVEA – Perú. Lima, Perú, June 26-28. Oviedo Rondón, E.O. 2014a. Effects of hatchery and incubation management on broiler performance, bone development and welfare. In Proceedings of ACPV Workshop From Eggs to Meat: Production of Quality Poultry Products. Clarion Resort Fontainebleau Hotel, Ocean City, MD. October 6-7. Oviedo Rondón, E.O. 2014b. Fatores que interferem no desenvolvimento embrionário e impactam no metabolismo do frango. In Proceedings of X Simpósio Técnico ACAV. Camboriú, Santa Catarina, Brasil, Septiembre 16-18. Oviedo-Rondón, E.O. 2012b. Buenas condiciones durante la incubación son claves para la salud y desempeño de los pollos. Avicultores y su Entorno. México. Memorias Seminario Internacional de Incubación y Producción de Pollos de engorde -‐ AMEVEA Oviedo-Rondón, E.O. 2012c. Considere la incubación en los programas de salud aviar. Industria Avícola. Septiembre. p. 20-25. Oviedo-Rondón, E.O. 2014c. Como mejorar la calidad del pollito? aviNews Febrero 2014, p. 24-34. Oviedo-Rondón, E.O. and M.J. Wineland. 2011. Incubation distress easily leads to splayed legs. World’s Poultry. Oznurlu Y., I. Celik., T. Telatar, y E. Sur. 2010. Br. Poult. Sci. 51(1):43-51. Tazawa, H., Y. Chiba, A. H. Khandoker, E. M. Dzialowski, and W. W. Burggren. 2004. Early development of thermoregulatory competence in chickens: Responses of heart rate oxygen uptake to altered ambient temperatures. Heart function, circulation and respiration in embryo and hatching. Pages 166–176 in Avian and Poultry Biology Reviews, Fundamental Physiology and Perinatal Development in Poultry. B. Tzschentke, and O. Janke, ed. Sci. Rev. Inc., Chicago, IL. Wineland M.J. y E. O. Oviedo-Rondón, 2009. Industria Avícola. Watt Publishing February 56 (2): 14-16. Yalçin, S., and P. B. Siegel. 2003. Exposure to cold or heat during incubation on developmental stability of broiler embryos. Poult. Sci. 82:1388–1392. Memorias Seminario Internacional de Incubación y Producción de Pollos de engorde -‐ AMEVEA
© Copyright 2026